Occorre innanzitutto chiarire che la corrosione galvanica è solo una delle tante forme di corrosione alle quali potrebbero essere soggette le reti di tubazioni metalliche e in particolare essa è tipica delle reti in cui siano utilizzati materiali diversi (solitamente, ma non necessariamente rame e ferro) senza prendere le opportune precauzioni. Questo meccanismo di corrosione si innesca quando in tali reti circola l’acqua e tra i materiali che la costituiscono (rame e ferro nel nostro caso, che hanno valori di nobiltà elettrochimica diversi) si instaura una circolazione di microcorrenti elettriche (effetto galvanico).
La corrosione
Nei punti in cui i due materiali vengono a contatto (giunzioni filettate, saldature, etc.) si forma così una vera e propria micropila elettrica in cortocircuito nella quale gli elettrodi sono costituiti dai due materiali stessi. Tra di essi si genera quindi un flusso di elettroni dal materiale meno nobile (il ferro nel nostro caso), che funge da polo negativo il quale si ossida cedendo materiale, verso quello più nobile avente potenziale maggiore (il rame nel nostro caso), che funge da polo positivo. Il flusso di elettroni provoca un vero e proprio “trasporto” sul polo positivo di materiale che viene sottratto da quello negativo.
Quindi in presenza di coppie galvaniche le tubazioni realizzate con il materiale meno nobile finiranno per corrodersi fino a cedere del tutto in prossimità delle zone di accoppiamento con le tubazioni realizzate in materiale più nobile.
A titolo di curiosità precisiamo che il complesso di reazioni chimiche che avviene durante la corrosione galvanica, sul quale non ci dilungheremo per non annoiare il lettore, ha il nome di “Redox” che deriva dalla contrazione dell’allocuzione anglosassone “Reduction and oxidation” (cioè “Ossidoriduzione”).
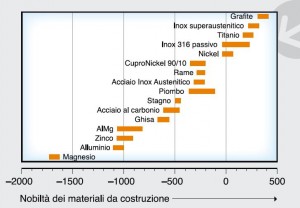
L’intensità dell’entità della corrosione dipende dalla differenza di potenziale che si crea tra i due elementi del dipolo elettrico, che è tanto più grande quanto più è diversa la nobiltà (o più tecnicamente la “Elettronegatività”) (vedere la figura 1) dei metalli che costituiscono il dipolo e dalla quantità di ossigeno che è dissolta nell’acqua.
La prevenzione o il contenimento della corrosione galvanica possono essere realizzati evitando il contatto tra materiali di nobiltà diversa isolando elettricamente materiali metallici differenti. Anche l’impiego di rivestimenti protettivi o di inibitori può ridurre il rischio di corrosione per contatto.
L’inserimento di giunti dielettrici
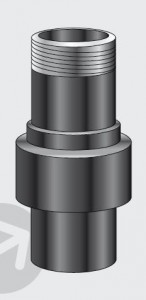
Per l’esecuzione delle rete tubiere miste l’accorgimento principe da adottare per prevenire la corrosione galvanica è costituito dall’inserimento di giunti dielettrici tra tubi in metalli diversi. In tal modo è possibile “interrompere” le micropile che viceversa si formerebbero ed impedire la circolazione delle microcorrenti prevenendo la corrosione delle tubazioni realizzate con il meno meno nobile tra i due metalli.
I giunti dielettrici per tubazioni metalliche (Figura 2) che dovrebbero essere utilizzati per la prevenzione della corrosione galvanica sono di solito costituiti da un tronchetto tubolare in acciaio completamente rivestito di materiale isolante. Poiché sono caratterizzati da una resistenza elettrica di almeno 5 MOhm, tali giunti sono di fatto in grado di isolare elettricamente i due metalli e di impedire quindi ogni circolazione di corrente tra di essi.